研究揭示乙肝相关慢加急性肝衰竭(ACLF)进展新机制


近日,中山大学器官移植中心何晓顺、郭志勇教授团队联合中山大学生命科学院邝栋明教授团队在国际知名期刊《肝病学》(Hepatology)上发表了一项新研究,揭示了乙型肝炎病毒(HBV)相关慢加急性肝衰竭(ACLF)病理进展的全新机制。该研究发现,肝细胞焦亡是HBV相关ACLF患者病理过程中最主要的细胞死亡模式,同时发现了一系列与焦亡相关的关键分子和信号路径,为改善这一致命性疾病的治疗提供了新的可能性。
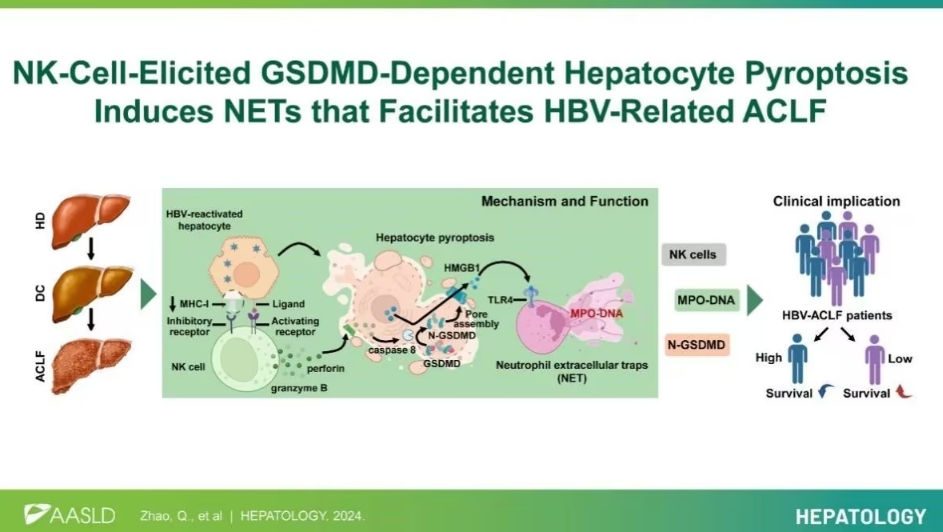
肝细胞焦亡是ACLF病理进展的关键
通过对正常肝组织、HBV相关肝硬化组织以及ACLF患者肝组织的转录组测序和组织原位染色分析,研究团队发现,肝细胞焦亡是HBV相关ACLF患者组织中主要的细胞死亡模式。焦亡是一种高度炎性形式的细胞死亡,其通过释放炎性因子加剧了肝脏损伤。
NK细胞介导的穿孔素/颗粒酶机制触发焦亡
机制研究显示,HBV的复燃激活导致肝细胞丢失MHC-I信号,从而被细胞毒性自然杀伤细胞(NK细胞)识别。研究证实,NK细胞通过穿孔素/颗粒酶依赖路径触发GSDMD和Caspase-8的激活,这一过程最终导致了肝细胞的焦亡。此外,焦亡过程中释放的HMGB1(高迁移率族蛋白B1)在加剧病变中起到关键作用。
HMGB1诱导中性粒细胞聚集及NETs形成
在焦亡肝细胞周围,中性粒细胞表现出高度选择性聚集。研究发现,焦亡细胞释放的HMGB1能够诱导周围聚集的中性粒细胞产生中性粒细胞胞外诱捕网(NETs)。NETs的形成被证实与肝内炎症环境恶化及病情进展密切相关,为乙肝相关ACLF的进一步恶化提供了重要线索。
MPO-DNA:NETs血浆标记物与患者预后的新指标
研究团队在HBV相关ACLF患者外周血样中分析了NETs标记物MPO-DNA的水平,并发现该指标与患者的预后密切相关。患者血浆中MPO-DNA水平越高,其预后越不理想,这标志着MPO-DNA可能成为评估患者病情和临床结局的重要预后标志物。
机械灌注模型验证治疗潜力:阻断GSDMD焦亡
研究团队还通过独特的常温机械灌注支持技术,建立了体外病肝养护模型。实验中,抑制肝细胞的GSDMD依赖性焦亡及HMGB1的释放,显著阻断了NETs的生成过程,从而有效遏制了HBV相关ACLF的病情进展。这一发现为靶向GSDMD焦亡通路以及调节相关免疫环境提供了新的治疗思路。
新研究的意义与未来方向
该研究的成果为理解HBV相关ACLF的病理机制提供了突破性洞见,并揭示了肝细胞焦亡及其调控的关键作用。它不仅提出了MPO-DNA作为评估预后的一种新型生物标志物,还提出了通过靶向焦亡及相关免疫干预的创新治疗策略。
未来,选择性调节GSDMD依赖的焦亡以及优化免疫微环境或将成为改善ACLF患者肝功能的重要方向。这一研究也为深入探索包括慢性肝病在内的其他炎性疾病的靶向治疗提供了新理论基础。