翰森制药伊奈利珠单抗获批新适应症:治疗IgG4-RD的突破性进展


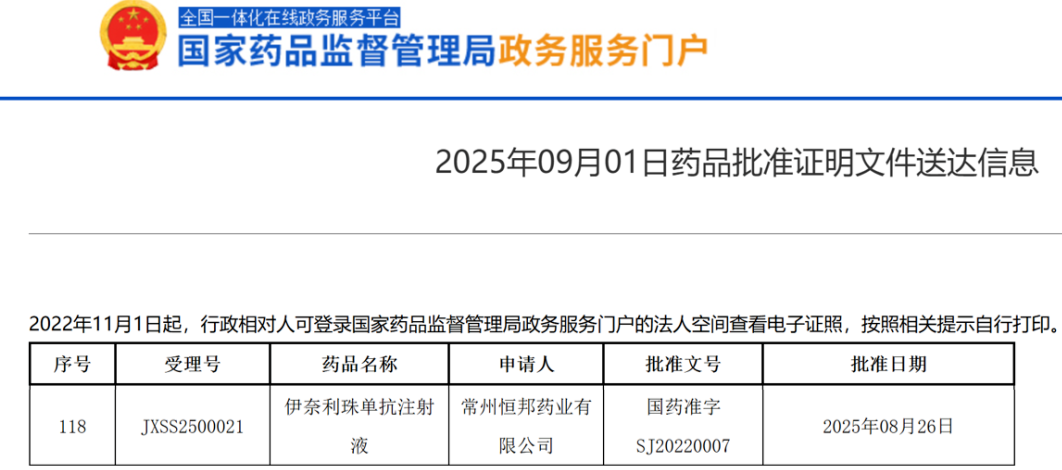
2025年9月1日,翰森制药宣布其子公司常州恒邦药业的伊奈利珠单抗(inebilizumab)获得国家药监局(NMPA)批准,正式进入免疫球蛋白G4相关疾病(IgG4-RD)成人患者的治疗适应症。伊奈利珠单抗成为全球首个获批治疗IgG4-RD的药物,标志着治疗该疾病领域的一项重要突破。
伊奈利珠单抗的背景与开发历程
伊奈利珠单抗是一种抗CD19单克隆抗体,最早由Viela Bio公司开发,并于2020年在美国首次获批。该药物主要用于治疗抗水通道蛋白4(AQP4)抗体阳性的视神经脊髓炎谱系障碍(NMOSD)成人患者。2022年,伊奈利珠单抗也获得了中国药监部门的批准,用于治疗此类患者。2019年,翰森制药与Viela Bio达成合作协议,获得了该药物在中国的开发与商业化权益。
III期MITIGATE研究:验证伊奈利珠单抗治疗IgG4-RD的疗效
2024年6月,伊奈利珠单抗在治疗IgG4-RD方面取得了重大进展。MITIGATE研究是一项III期临床试验,旨在评估该药物对IgG4-RD的疗效与安全性。该试验为随机、多中心、双盲、安慰剂对照的设计,纳入了160名患者,治疗期为52周。
研究结果表明,在接受伊奈利珠单抗治疗的患者中,IgG4-RD发作风险相比安慰剂组降低了87%(HR=0.13,p<0.0001)。该药物还显著改善了年化发作率和完全缓解率(无发作、免治疗)。此外,研究还未发现新的安全性问题,进一步确认了伊奈利珠单抗的安全性和耐受性。
IgG4-RD的挑战与治疗前景
IgG4-RD是一种免疫介导的慢性全身性疾病,通常会导致多个器官的炎症和纤维化,进而造成不可逆的器官损伤。此疾病的发病率估计约为1/100,000到5/100,000。CD19阳性B细胞在IgG4-RD的发生中起着关键作用,驱动疾病的炎症和纤维化过程。当前,全球仅有伊奈利珠单抗和obexelimab正在进行针对IgG4-RD的III期临床试验。
未来展望:IgG4-RD治疗的创新
伊奈利珠单抗的获批为治疗IgG4-RD患者提供了新的希望。随着这一药物的上市,治疗IgG4-RD的治疗方案将不再局限于传统的免疫抑制药物,患者将能从更精确和高效的治疗中获益。此外,MITIGATE研究的成功为未来相关药物的研发提供了重要的参考,进一步推动了免疫治疗在罕见疾病领域的应用。
总结:伊奈利珠单抗开创IgG4-RD治疗新纪元伊奈利珠单抗的获批,不仅代表了治疗IgG4-RD的新选择,更为免疫疾病的创新治疗提供了示范。随着这一药物在中国市场的上市,预计将为大量IgG4-RD患者带来更为有效的治疗方案,推动这一领域的医学进步。