300亿白蛋白市场迎来变革:国产重组人白蛋白新药首获批


7月18日,国家药品监督管理局(NMPA)公告,武汉禾元生物科技股份有限公司开发的重组人白蛋白注射液(水稻)(商品名:奥福民)正式获批上市。本品适应症为用于治疗肝硬化低白蛋白血症(≤30g/L),这一批准标志着国产白蛋白研发迎来了历史性突破。
白蛋白:难以替代的“黄金救命药”
白蛋白由于其特殊的生理功能,被广泛应用于多种危重病症的治疗,例如肝硬化腹水、烧伤、手术后的体液补充,以及因失血过多导致的低血容量性休克。
市场数据显示,仅2023年和2024年,国内白蛋白终端销售额分别高达 344亿元 和 300亿元,需求量持续增长。
然而,人血清白蛋白来源严重依赖血浆提取,这一传统工艺带来了以下问题:
血浆资源短缺:我国血浆供应长期受限,生产能力有限;
依赖进口:进口产品在供应中占据了绝大比例;
高成本与可及性受限:昂贵的成本和有限的可获得性,令患者面临“救命药”短缺的困境。
“稻米造血”:国产技术实现历史性突破
为解决这些困境,禾元生物提出了“稻米表达技术新方案”,这一技术曾被视为天方夜谭,但现已成为现实。具体而言,团队通过基因工程将人白蛋白基因导入水稻种子,使水稻胚乳细胞能够表达目标蛋白。该技术的核心平台包括:
OryzHiExp:水稻高效重组蛋白表达系统;
OryzPur:水稻蛋白纯化技术平台。
相比传统血浆提取方法及酵母表达体系,水稻表达体系具备以下显著优势:
安全性高:完全无血源性疾病传播风险;
免疫原性低:更符合患者需求;
成本低、生产环保:有效降低生产成本且绿色环保。
临床试验数据证明其安全性与有效性
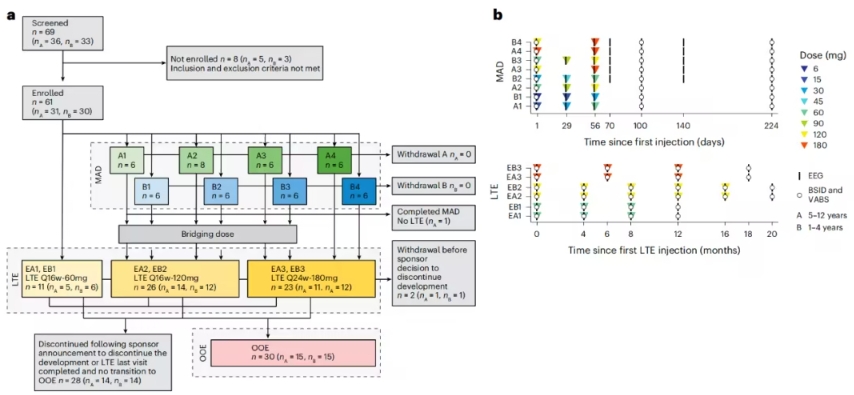
2024年11月,禾元生物公布HY1001(奥福民)在肝硬化低白蛋白血症患者中的Ⅲ期关键临床试验数据:
疗效不劣于进口产品:HY1001按剂量20g/天、最长治疗14天,其血清白蛋白的提升效果与传统的人血浆来源白蛋白(pHSA)相当;随访期内疗效稳定。
安全性佳:试验数据表明患者对HY1001耐受性良好,不良反应率低于预期。
商业化进展:产能扩大加速布局
为了保障商业化供应,禾元生物已构建起强大的生产能力布局:
已建成一座年产10吨原液(100万瓶注射液)的智能化工厂,并获得药品生产许可证;
未来武汉光谷生产基地可实现年产120吨原液(1200万瓶注射液),计划于2026年投产;
公司与贝达药业达成战略合作,后者将独家负责HY1001在中国市场的商业推广。
IPO助力发展:24亿元资金聚焦产业化
为了进一步扩展其生产能力和市场布局,禾元生物已经向科创板提交IPO申请,计划发行近 9000万股,募资金额约 24亿元。其中重点项目为——重组人白蛋白产业化基地建设项目,预计将为其规模化生产奠定坚实基础。
结束进口依赖,国产白蛋白迎来新里程碑
此次HY1001的成功获批上市,不仅是禾元生物技术突破与研发实力的体现,更是我国白蛋白市场的一次重要革新。该药的上市有望从根本上缓解国内对进口产品的依赖,并为肝硬化患者提供一种更安全、可负担的治疗选择。
随着水稻重组人白蛋白技术进入临床应用,这一具有革命性意义的国产创新药将在未来持续造福更多患者,为生命健康事业注入全新动力。