礼来塞普替尼新适应症获NMPA受理:覆盖RET融合实体瘤儿童患者


2025年8月15日,国家药品监督管理局(NMPA)药品审评中心(CDE)官网显示,礼来的塞普替尼(Selpercatinib)新适应症上市申请已正式获受理。根据注册性临床研究的进展推测,此次申报的适应症可能针对RET基因融合的局部晚期或转移性实体瘤儿童患者,这一进展为RET相关肿瘤治疗打开了新的篇章。
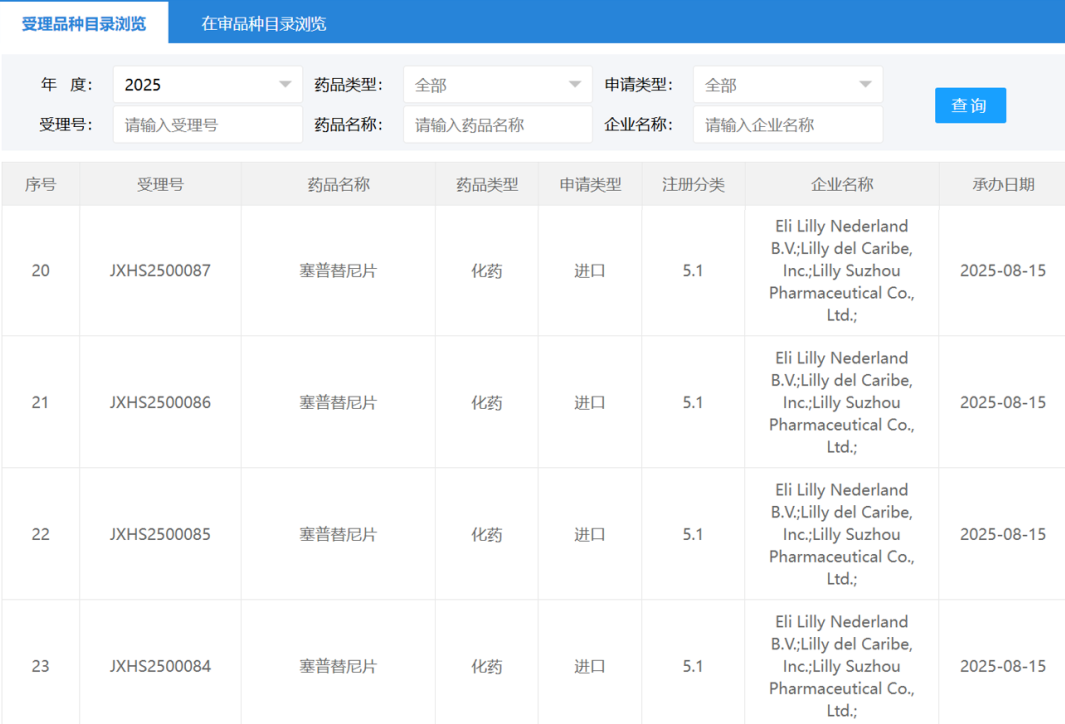
塞普替尼:全球首个高选择性RET抑制剂
药物简介
塞普替尼是一种强效、高选择性、口服RET酪氨酸激酶抑制剂,专门针对RET基因融合或突变相关的肿瘤。该药物具有精准靶点作用机制,通过有效抑制RET激酶的异常活化,显著抑制肿瘤的生长和扩散。
全球获批历史
2020年5月:塞普替尼成为全球首个获FDA批准的高选择性RET抑制剂,用于治疗RET融合阳性非小细胞肺癌(NSCLC)和RET突变型甲状腺相关肿瘤。
2022年10月:国内正式获批,用于非小细胞肺癌、**RET突变型甲状腺髓样癌(MTC)以及RET融合阳性甲状腺癌(TC)**的成人和12岁及以上儿童患者。
聚焦新适应症:RET融合实体瘤儿童治疗
LIBRETTO-121研究结果支撑
塞普替尼的新适应症得到了最新临床研究数据的有力支持。一项I/II期临床试验(LIBRETTO-121研究)专门针对带有RET基因改变的晚期实体瘤或神经系统原发性肿瘤的儿科患者,结果显示:
中位随访30个月,可评估患者(n=36)客观缓解率(ORR)为36%;
24个月持续缓解率(DOR)为100%,进一步印证了疾病控制的持久性;
24个月无进展生存率(PFS)高达86%。
分患者群体疗效
在研究中,不同RET相关肿瘤患者的表现均显著:
RET突变型甲状腺髓样癌患者(n=15):ORR为40%,疗效显著稳定;
RET融合阳性甲状腺癌患者(n=15):ORR为33.3%,同样展现较好的疾病缓解率。
这一数据支持塞普替尼未来更加广泛适用于儿童实体瘤患者的可能性,为RET相关肿瘤治疗提供了新选择。
RET融合:治疗性靶点的重要性
RET基因改变概述
RET基因的突变或融合是多种实体瘤的重要驱动因素,尤其在非小细胞肺癌(NSCLC)、甲状腺髓样癌(MTC)和甲状腺癌(TC)中广泛存在。
RET融合特别影响儿童患者
在儿科实体瘤中,RET融合或突变同样是重要的病因,而针对儿童患者的治疗选择较为有限。塞普替尼通过高选择性靶向RET激酶,为疾病控制提供了精准医学的新实践。
临床意义与未来展望
塞普替尼的最新进展提供了哪些意义?
儿童群体治疗突破
此次新适应症受理表明,塞普替尼有望填补儿童RET融合实体瘤治疗的空白,尤其是在中晚期无有效治疗手段的情况下,为这些患者提供疾病改善的可能。
长效控制与耐受性良好
临床研究显示长期治疗效果显著,帮助延长患者无进展生存期(PFS)并提供持续缓解。同时,塞普替尼口服给药的方式改善了儿童患者的用药便利性。
精准医学的进一步推进
塞普替尼的成功验证了RET作为关键靶点的临床价值,并进一步巩固了其在个性化治疗领域的领先地位。
未来发展方向
适应症覆盖扩展:未来可以探索塞普替尼在更多RET基因相关肿瘤类型中的应用;
全球布局与推广:加强市场推广与国际合作,让更多患者受益于精准的RET靶向治疗;
联合疗法研究:结合免疫治疗或其他靶向药物,进一步优化治疗方案,提升疗效。
总结
礼来的塞普替尼作为全球首个RET抑制剂,凭借其高选择性和强效性,在RET相关肿瘤治疗领域已经取得卓越成绩。此次新适应症获NMPA受理,意味着其即将在儿童RET融合实体瘤治疗中发挥更大的作用,为更多患者提供更加精准和有效的治疗方案。未来,随着更多临床数据的积累和新适应症的拓展,塞普替尼有望在抗肿瘤领域继续保持领先态势,为全球患者带来更多的生命希望。