瑞吉生物冻干mRNA结核病疫苗RH119获临床试验申请受理,抗结核领域迎来新突破


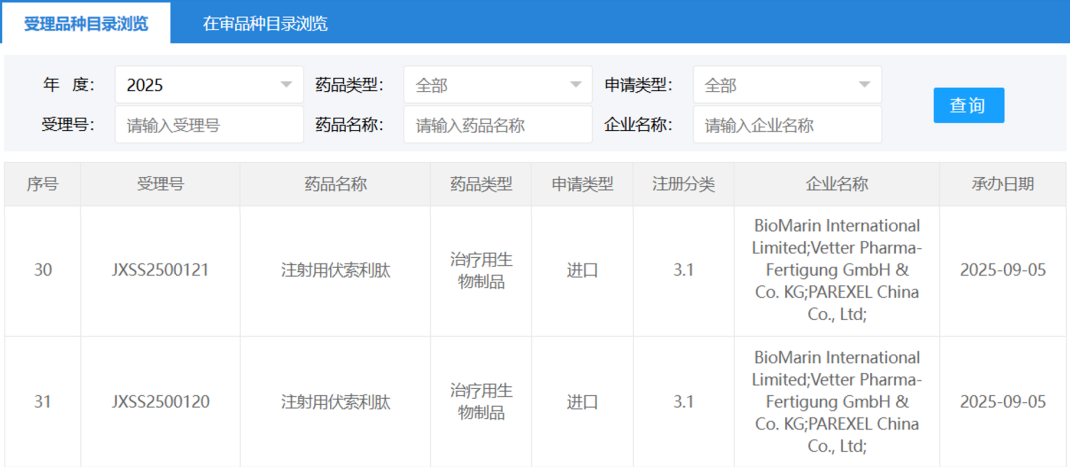
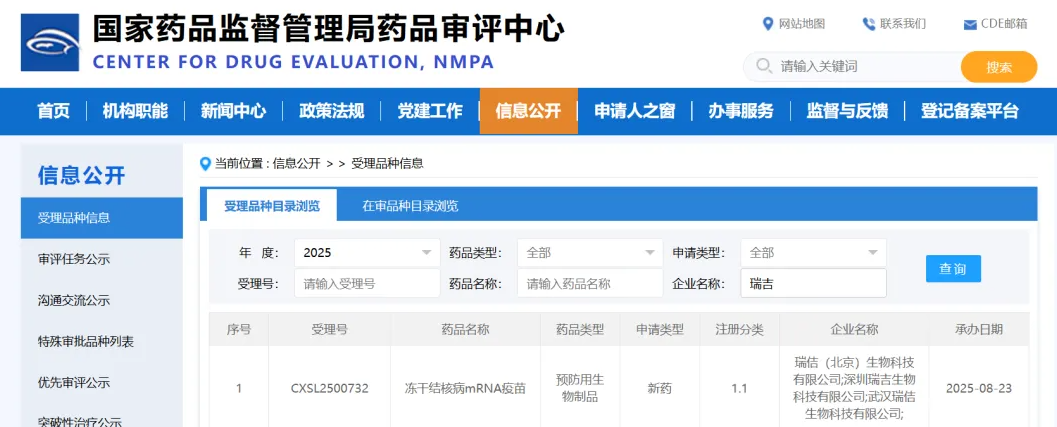
近日,国家药品监督管理局药品审评中心(CDE)官网公示显示,由瑞吉生物申报的“冻干结核病mRNA疫苗RH119”新药临床试验申请(IND)已获CDE受理(受理号CXSL2500732)。这一疫苗是瑞吉生物拥有自主知识产权并全球首创的冻干型结核病mRNA疫苗,申报注册分类为1.1类(指针对无有效预防手段疾病的创新疫苗)。此举标志着我国在结核病疫苗开发领域实现了重要突破,为全球结核病防治带来新的希望。
结核病:全球公共卫生挑战的严峻现状
结核病作为全球最严重的传染性公共卫生问题之一,每年导致大量疾病和死亡。据统计,全球约四分之一人口感染结核分枝杆菌,每分钟平均约有2至3人因结核病失去生命。尽管结核病防治工作取得了显著进展,但目前仍面临巨大挑战,尤其是针对潜伏感染人群及青少年、成年患者的有效防控方案尤为稀缺。
从1921年开始,BCG疫苗(卡介苗)成为结核病防治的重要工具,它通过减毒的牛结核分枝杆菌培养而成,对婴幼儿播散性结核病具有良好的保护作用。然而,BCG疫苗的保护效力具有显著局限性——保护效果仅持续15年,并随着接种时间延长逐渐减弱,对青少年及成年人群的防护能力有限。因此,急需开发针对所有年龄段的更有效、更持久的疫苗。
mRNA技术:传染病防控的革命性突破
新冠疫情期间,mRNA疫苗在病毒防治领域表现出非凡潜力,其机制通过将编码病原体目标蛋白的信使RNA(mRNA)递送到机体细胞内,刺激免疫应答,提供疾病保护。目前,mRNA技术已在细胞病毒性疫苗方面取得广泛成功,而国际科研团队在细菌mRNA疫苗领域的探索亦取得突破性进展。例如,以色列特拉维夫大学和生物研究所开发的全球首款抗细菌mRNA疫苗,用于防控高致死性鼠疫耶尔森菌,成为标志性成果。
RH119:国产mRNA疫苗开启结核病防控新篇章
瑞吉生物基于mRNA技术,开发出了全球首款冻干型结核病mRNA疫苗——RH119。这款疫苗涵盖了多种结核分枝杆菌关键抗原组合,旨在进一步增强免疫应答并提高对不同群体的保护效果。冻干制剂形式既提升了疫苗的稳定性和保存条件,也更适合在复杂公共卫生环境中推广。
2025年1月和3月,瑞吉生物已分别在武汉金银潭医院与北京胸科医院启动了两项研究者临床试验(IIT),分别针对健康人群和潜伏感染人群,推动RH119的早期临床数据收集。这些研究试验是开发适用于不同风险人群的创新结核病疫苗的重要一步。
影响力与未来前景:全球防治结核的新希望
RH119疫苗临床试验获受理不仅体现了瑞吉生物在结核病防治领域的技术创新能力,也为破除传统疫苗局限提供了新的可能:
对潜伏感染人群的覆盖:RH119预计能够填补现阶段疫苗无法有效预防潜伏结核感染的空白,改善预防效果。
全龄段保护潜力:覆盖健康人群及成人感染群体,有望显著减少结核病传播,改善重症治疗困境。
冻干形式优势:延长疫苗储存期,简化运输和应用条件,将极大提升疫苗在全球范围内的供应保障能力。
总结
作为全球首款冻干型结核mRNA疫苗,RH119获得CDE临床试验受理标志着我国mRNA技术进入了抗结核细菌疫苗的新领域。瑞吉生物通过积极开展临床研究,探索疫苗适用范围,为全球结核病防治提供了创新疗法。未来,随着RH119临床试验的深入推进,我们有望见证一款兼具高效性、安全性和便利性的革命性疫苗问世,为全球数亿结核病患者乃至潜伏感染者带来福音,同时彰显中国生物医药技术在国际舞台上的核心竞争力。