全球首个HER2靶向药:宗艾替尼正式获批,为晚期非小细胞肺癌患者带来新希望


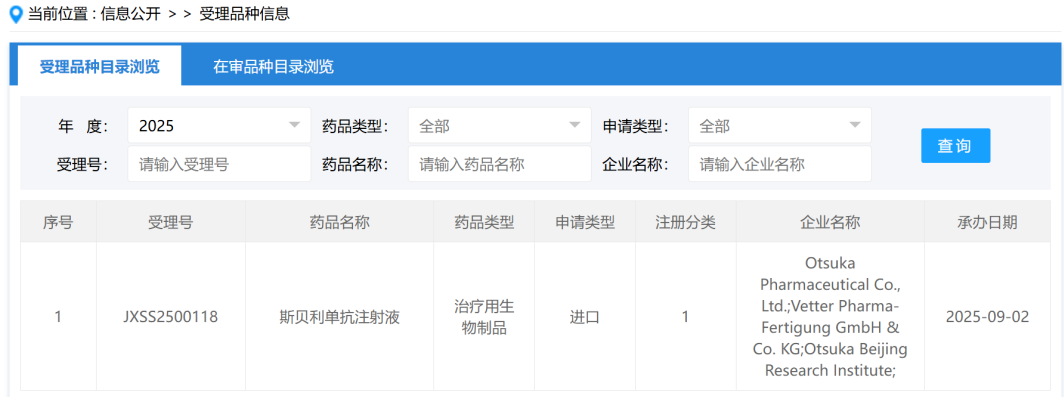
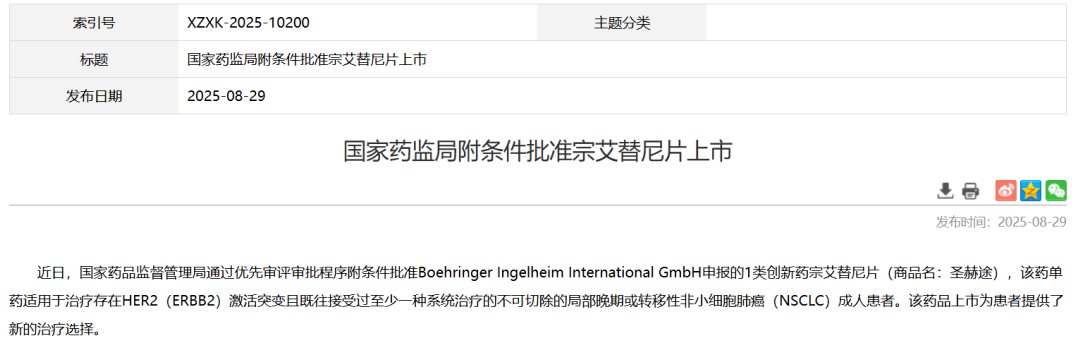
8月29日,国家药品监督管理局(NMPA)官网显示,勃林格殷格翰开发的宗艾替尼片(Zongertinib)已经获得上市申请的批准。这款药物针对不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者,治疗对象需具有HER2(ERBB2)激活突变且既往接受过至少一种系统性治疗。宗艾替尼是全球范围内首个,也是目前唯一获批的口服HER2酪氨酸激酶抑制剂(TKI),为肺癌治疗领域提供了新的解决方案。
宗艾替尼的精准机制:高选择性HER2靶点抑制药物
宗艾替尼(研发代号:BI 1810631)通过与HER2受体(野生型及突变型,包括携带外显子20突变)中的酪氨酸激酶结构域(TKD)形成共价结合,从而实现强效抑制。相比传统治疗方案,宗艾替尼对HER2的选择性更高,有望提供更优的疗效及更好的患者耐受性。这一机制创新不仅突显了勃林格殷格翰在肿瘤靶向药物研发领域的能力,也为患有该类型HER2突变的NSCLC患者带来了期待已久的治疗新选择。
战略合作推动药物商业化落地
2024年4月,勃林格殷格翰与中国生物制药达成战略合作。双方通过资源共享和优势互补,共同致力于在中国内地开展BI肿瘤学药物的研发和商业化工作,其中宗艾替尼作为重点布局品种之一,未来将在中国市场发挥更大作用。这一合作将加速宗艾替尼在国内的推广,同时拓展其惠及患者的广度和深度。
HER2突变NSCLC患者急需新疗法
数据显示,我国患有NSCLC的患者中,HER2基因突变的比例约为2%-4%。然而,与其他基因变异的NSCLC类型相比,HER2突变患者的预后更差,其中位总生存期(OS)仅为1.6-1.9年,与拥有EGFR突变或ALK/ROS1重排的NSCLC患者相比无进展生存期(PFS)也更短。针对这类患者的治疗需求,宗艾替尼的出现无疑是一个里程碑,可显著改善患者的生存与生活质量。
基于Beamion LUNG-1研究获批:临床数据有力支持
此次NMPA批准宗艾替尼的上市,是基于Beamion LUNG-1研究Ia/Ib期的积极研究结果。在队列1中,针对已经接受过治疗的HER2突变患者(n=75),宗艾替尼展现出优秀的疗效指标:客观缓解率(ORR)达71%,其中7%实现完全缓解(CR),疾病控制率(DCR)则高达96%。此外,中位缓解持续时间(DoR)为14.1个月,中位无进展生存期(PFS)为12.4个月。这些数据表明宗艾替尼对HER2阳性NSCLC患者具有显著的疗效,同时其安全性极为可控,治疗中断率在研究中仅为2.9%。
展望未来:HER2精准治疗技术的突破与前景
宗艾替尼作为首个获得批准的HER2 TKI药物,在针对HER2阳性的NSCLC患者中显示了卓越疗效,也为这一领域的精准治疗开创新的范式。凭借数据支持和战略合作,宗艾替尼不仅为晚期肺癌患者带来生存希望,同时也推动了中国在肿瘤精准治疗领域的进步。
勃林格殷格翰与中国生物制药的深度合作,以及国家药监局对创新药物的积极审批,将进一步扩大宗艾替尼在中国市场的使用场景,为更多HER2突变肺癌患者提供救命选择。未来,期待这一药物为治疗难治性肺癌提供持久支持,同时推动全球肿瘤治疗技术迈向新高度。