国家药监局批准新冠口服药“奥格特韦钠”附条件上市


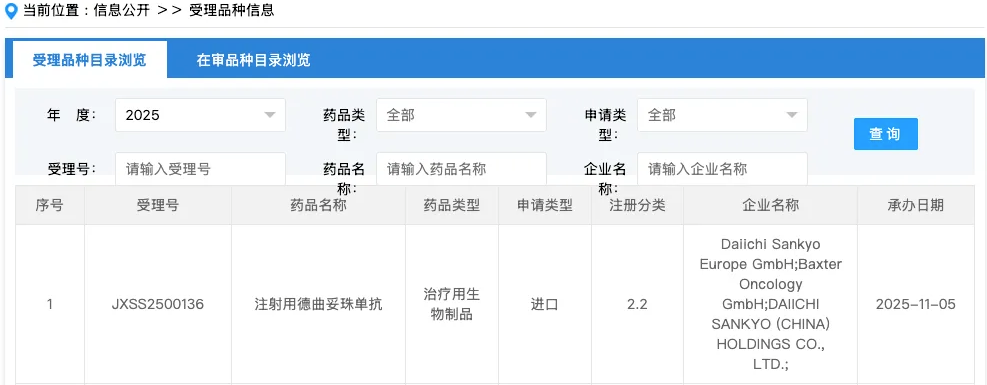
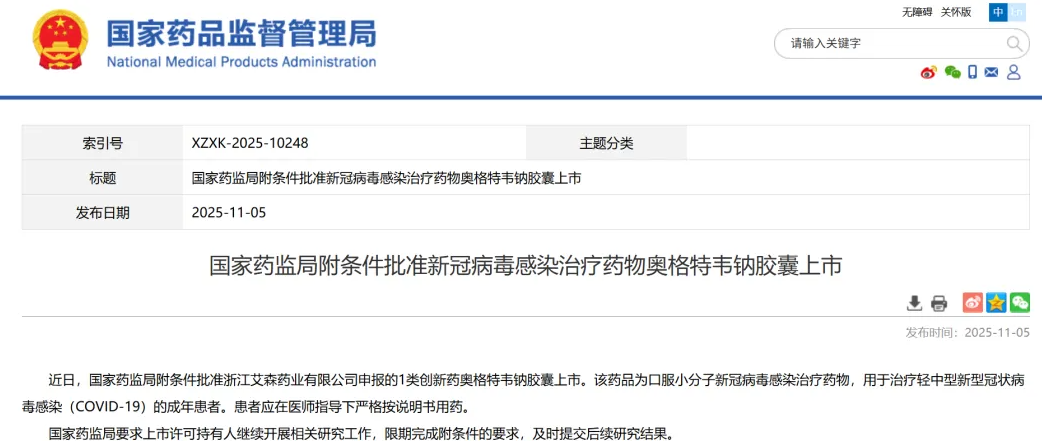
11月5日,国家药品监督管理局正式发布消息,批准浙江艾森药业有限公司研发的1类创新药——奥格特韦钠胶囊附条件上市。这意味着我国在新冠病毒感染治疗领域的药物研发又取得了重要进展。
口服小分子药物,聚焦轻中度患者
奥格特韦钠胶囊是一种口服小分子抗病毒药物,主要用于治疗轻度至中度的新型冠状病毒感染(COVID-19)成人患者。该药通过抑制病毒复制过程中的关键酶活性,从而有效阻止病毒扩散,有望缩短病程、减轻症状并降低疾病进展风险。
“附条件批准”意味着什么?
根据国家药监局的公告,本次批准属于附条件上市,即在初步临床数据证明药物疗效和安全性可接受的前提下,允许其尽早应用于临床,以满足紧迫的公共卫生需求。企业仍需持续开展相关研究,完善后续临床试验数据。
国产抗疫药物研发进入新阶段
随着奥格特韦钠胶囊的上市,我国本土企业在新冠治疗药物领域实现了又一次突破。这不仅丰富了临床用药选择,也体现了我国在创新药物研发体系上的成熟与自信。
业内专家指出,国产口服抗病毒药物的不断问世,将为疫情防控和患者治疗提供更便捷、更具成本效益的解决方案。
结语:
奥格特韦钠胶囊的上市标志着我国在新冠药物自主研发领域迈出了坚实一步。未来,随着更多临床数据的积累,这款创新药有望在抗击新冠感染中发挥更大作用,为轻中度患者带来新的治疗选择。